Les instruments de l'invisible : Partie 4
Sciencylogie
AuteurAnne-Lise Cribier
Si les microscopes à sonde locale ont appris à « sentir » la matière à l’échelle nanométrique, une autre famille d’instruments pousse encore plus loin les limites de l’observation optique. Il s’agit des microscopes à super-résolution.
Pendant plus d’un siècle, voir le vivant revenait à composer avec une frontière que l’on pensait intangible. La limite de diffraction d’Abbe, autour de 200 nanomètres, fixait un seuil au-delà duquel les détails se diluent et la lumière perd sa capacité à distinguer.
Cette frontière a longtemps structuré la manière même d’observer la cellule. Puis, sans disparaître, elle a commencé à être contournée, déplacée, repoussée.
Les techniques de super-résolution permettent aujourd’hui de descendre entre 10 et 100 nanomètres selon les approches. À cette échelle, la cellule change de visage. Les grandes structures restent visibles, mais ce sont surtout les organisations fines qui apparaissent, celles des protéines, des membranes et des organites. Ce qui était implicite devient observable.
Ce basculement ne tient pas seulement à un gain de précision. Il marque une transformation plus profonde de la biologie, qui ne se limite plus à observer le vivant, mais apprend à en reconstituer les détails invisibles.
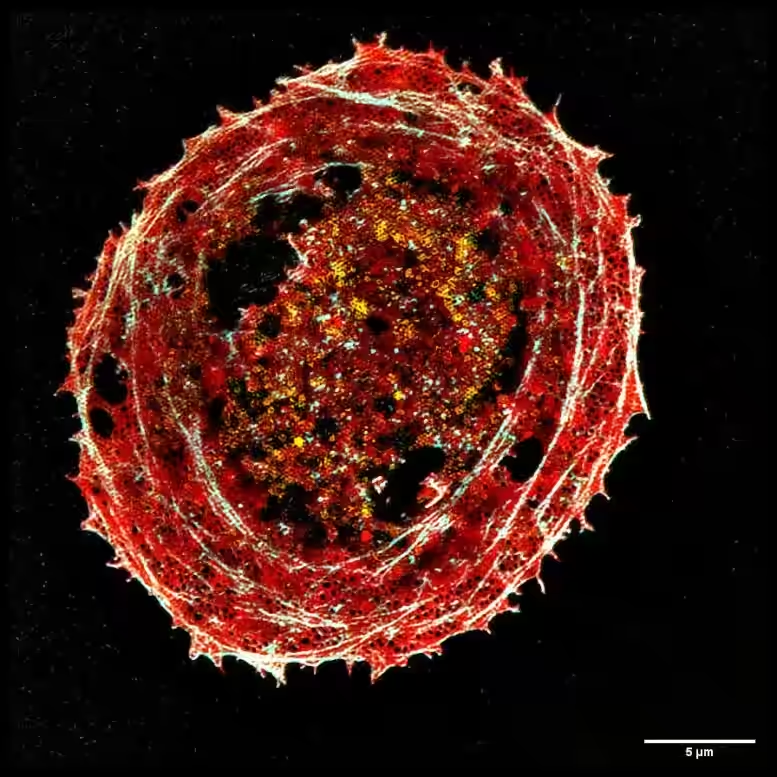
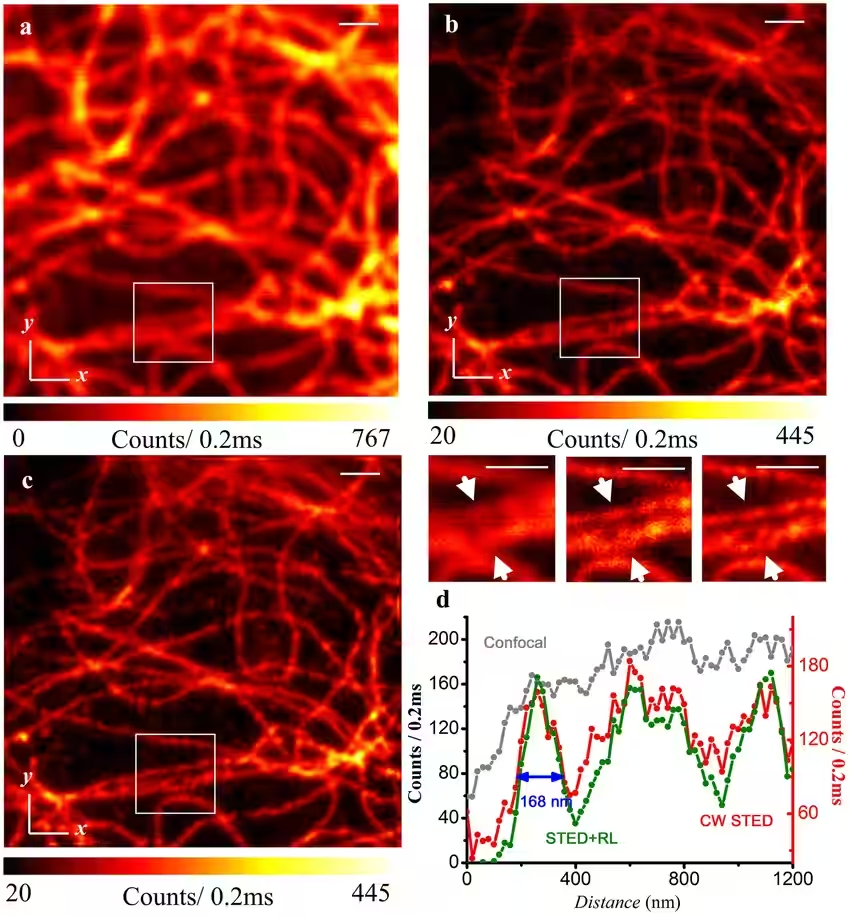
L’image montre de très petites structures situées dans les membranes des cellules, si petites qu’elles ne peuvent pas être distinguées avec un microscope optique classique. Crédit : Henning Ortkrass, Université de Bielefeld
Le STED : Sculpter la lumière par le vide
Le microscope à déplétion stimulée (STED, technique de microscopie optique à super-résolution qui réduit la zone fluorescente observée) ne se contente pas d’éclairer le minuscule. Il exploite les interactions entre lumière et matière au niveau moléculaire pour affiner son regard.
Son principe repose sur l’usage coordonné de deux lasers (sources de lumière cohérente amplifiée). Le premier excite les fluorophores (molécules fluorescentes capables d’émettre de la lumière après excitation) d’un point précis, comme dans un microscope classique. C’est alors qu’intervient le second laser, dit de « déplétion » (faisceau lumineux utilisé pour inhiber la fluorescence). Celui-ci utilise une impulsion lumineuse spécifique qui induit une émission stimulée (processus par lequel une molécule excitée est forcée de revenir à son état initial sans émettre spontanément de photon) : il force les fluorophores situés en périphérie du point à revenir à leur état fondamental (état énergétique le plus bas d’une molécule) avant toute émission spontanée de lumière.
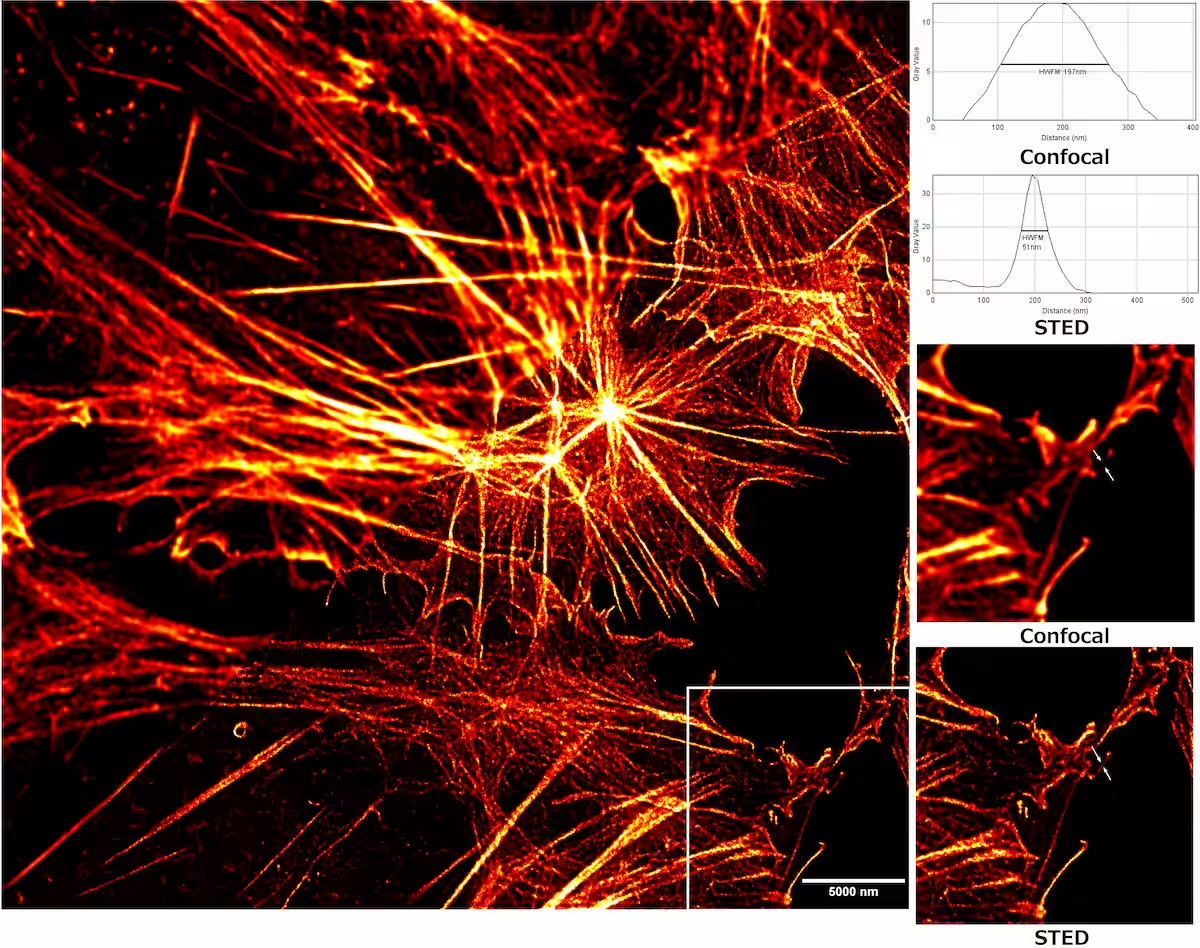
En « éteignant » ainsi la fluorescence autour du centre, seule une infime zone reste active. Ce procédé permet de visualiser des structures intracellulaires (structures internes des cellules vivantes) avec une précision de 20 à 30 nanomètres. Toutefois, cette performance reste un équilibre subtil : elle dépend étroitement de la nature des fluorophores, de l’intensité des lasers, du rapport signal/bruit (rapport entre le signal utile et les perturbations parasites) et de la stabilité rigoureuse du système d’imagerie (ensemble optique et mécanique assurant la constance des mesures).
L’image montre de très petites structures situées dans les membranes des cellules, si petites qu’elles ne peuvent pas être distinguées avec un microscope optique classique. Crédit : Henning Ortkrass, Université de Bielefeld
Anecdote : Le pionnier de la lumière domptée
Le physicien Stefan W. Hell a reçu le prix Nobel de chimie en 2014 pour ses travaux en microscopie optique à très haute résolution. En développant le STED (microscopie à émission stimulée par déplétion, technique qui réduit la fluorescence en dehors d’une zone focalisée), il a montré que la limite de diffraction (limite physique de résolution imposée par la nature ondulatoire de la lumière) n’était pas une fatalité. Ses travaux ont ouvert la voie à l’observation dynamique du vivant à l’échelle nanométrique (échelle du milliardième de mètre).
PALM et STORM : La symphonie des points isolés
Là où le STED (microscopie à émission stimulée par déplétion) réduit la zone éclairée, les microscopes PALM et STORM reconstruisent l’image à partir du chaos apparent des molécules.
Le secret réside dans l’activation stochastique (processus aléatoire gouverné par des probabilités) des molécules : on n’allume les fluorophores (molécules fluorescentes capables d’émettre de la lumière après excitation) que quelques-uns à la fois, de manière très clairsemée — une activation dite sparse (peu dense) et non chevauchée (sans superposition des signaux lumineux). En isolant chaque émetteur, on peut déterminer sa position avec une précision mathématique extrême avant de reconstituer l’image finale.
Bien que souvent citées ensemble, ces deux méthodes diffèrent par leurs outils :
- Le PALM (PhotoActivated Localization Microscopy, microscopie de localisation par photo-activation), dont les travaux ont valu le prix Nobel 2014 à Eric Betzig, utilise des protéines photo-activables (protéines dont la fluorescence peut être déclenchée par la lumière).
- Le STORM (STochastic Optical Reconstruction Microscopy, microscopie optique de reconstruction stochastique), développé par Xiaowei Zhuang à Harvard, s’appuie sur des fluorophores organiques (molécules fluorescentes non protéiques utilisées comme marqueurs).
Cette technique permet d’étudier des complexes protéiques (assemblages de protéines fonctionnelles dans la cellule) avec une résolution de 10 à 20 nanomètres. C’est un travail de patience : l’acquisition (processus de capture des données d’image) est lente car il faut répéter le processus des milliers de fois. C’est comme allumer des petites lucioles une par une pour dessiner, point par point, une image d’une précision absolue.
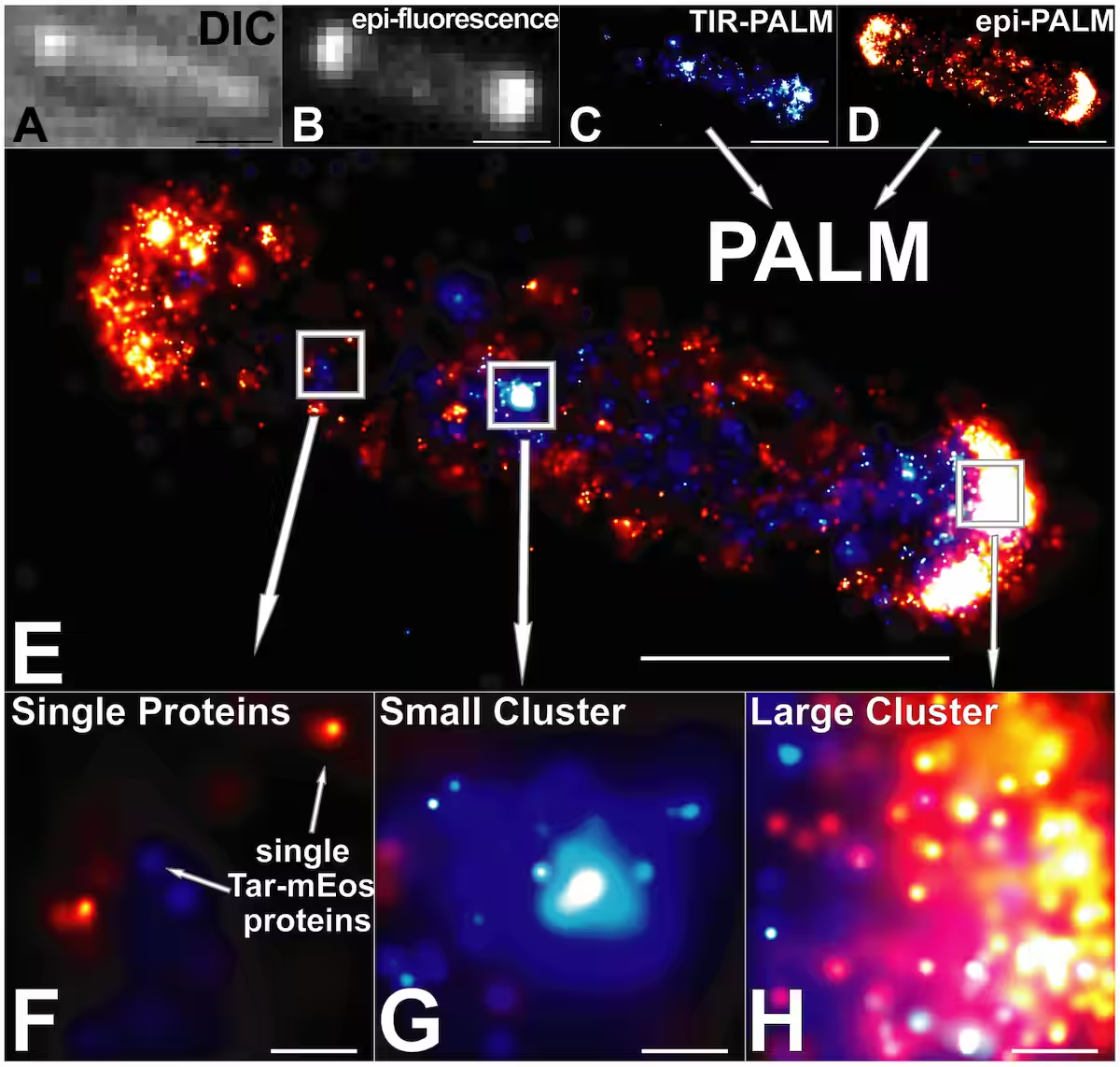
(A) Image d’une cellule unique en contraste interférentiel différentiel (DIC).
(B) Image en épifluorescence, limitée par la diffraction.
(C) Image PALM en illumination TIR. Chaque protéine est représentée par une distribution gaussienne 2D, dont la largeur reflète l’incertitude de localisation.
(D) Image PALM en épifluorescence, acquise après blanchiment des protéines Tar-mEos dans la zone TIR.
(E) Superposition des images (C) et (D).
(F) Zoom sur des protéines individuelles (n = 44) dans la zone encadrée à gauche de (E).
(G) Zoom sur un petit agrégat (n = 241) dans la zone centrale de (E).
(H) Zoom sur un grand agrégat polaire (n = 722) dans la zone encadrée à droite de (E).
Échelle :
(A–E) 1 µm
(F–H) 50 nm
Crédit : Greenfield D., McEvoy A. L., Shroff H., Crooks G. E., Wingreen N. S., Betzig E., Liphardt J., 14 juillet 2013.
Le SIM : L'intelligence des motifs
Le microscope à illumination structurée (SIM, technique d’imagerie qui utilise des motifs lumineux pour extraire des détails fins) mise sur une stratégie différente pour obtenir des images 3D à haute résolution spatiale.
Ici, l’échantillon est éclairé par des motifs lumineux sinusoïdaux (ondes périodiques en forme de vagues régulières, ici sous forme de “rayures”). L’interaction entre ces motifs et les structures fines de l’échantillon génère un « effet de moiré » (phénomène d’interférence visuelle créant des motifs apparents à partir de deux structures superposées). A l’aide d’un traitement informatique (ensemble d’algorithmes de calcul) complexe combinant plusieurs images prises sous différentes phases (décalages du motif lumineux), le microscope reconstruit les détails fins. Cette technique permet de dépasser la limite classique de diffraction (limite physique de résolution imposée par la nature ondulatoire de la lumière) jusqu’à environ 100 nanomètres.
Le SIM est l’outil de prédilection pour l’observation rapide des cellules vivantes (unités biologiques fondamentales des organismes vivants). Cependant, il reste moins fin que le STED ou le PALM/STORM. De plus, s’il permet d’explorer des échantillons volumineux (objets biologiques de grande taille en 3D), il perd en efficacité lorsqu’il s’attaque à des tissus trop épais où la diffusion (dispersion de la lumière dans le matériau) brouille les motifs lumineux. La puissance de calcul (capacité informatique nécessaire au traitement des données) requise impose un délai de traitement de 1 à 30 secondes avant d’obtenir l’image finale.
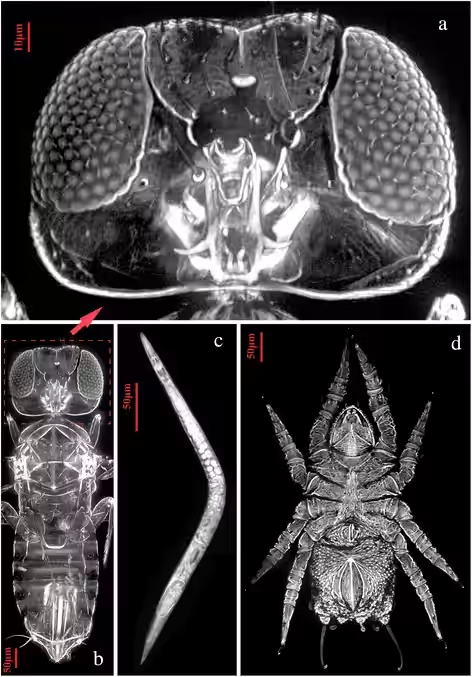
Images en microscopie LED-SIM de différents petits organismes.
(a) Détail de la tête d’Aphytis sp., agrandissement numérique de la zone encadrée en (b).
(b) Guêpe parasitoïde Aphytis sp., projection d’intensité maximale (98 images le long de l’axe Z), objectif 20×.
(c) Nématode Panagrellus redivivus, projection d’intensité maximale (26 images le long de l’axe Z), objectif 20×.
(d) Vue ventrale d’un acarien, projection d’intensité maximale (89 images le long de l’axe Z), objectif 20×.
Crédit : M. Ming Bai, Institute of Zoology, Chinese Academy of Sciences, juin 2016.
Le RESOLFT : La douceur du regard
Directement issu des travaux de Stefan Hell, le microscope RESOLFT peut être vu comme un cousin plus “prévenant” du STED (microscopie à émission stimulée par déplétion). Si l’objectif reste identique (réduire la zone d’émission lumineuse pour augmenter la résolution) la philosophie, elle, change radicalement.
Ici, il ne s’agit pas d’éteindre la fluorescence (émission de lumière par une molécule excitée) par la force d’un laser intense. Le RESOLFT repose sur des marqueurs fluorescents (molécules capables d’émettre de la lumière après excitation) dits “photoswitchables” (capables de changer d’état sous l’effet de la lumière), capables de fonctionner comme de véritables interrupteurs moléculaires. Au lieu d’un faisceau de déplétion (faisceau lumineux servant à forcer l’extinction de la fluorescence) puissant, on utilise une lumière beaucoup plus douce pour faire basculer ces molécules entre un état fluorescent (“allumé”) et non fluorescent (“éteint”).
Cette approche présente des avantages majeurs pour la biologie :
- Moins de lumière, plus de vie : en réduisant l’intensité lumineuse, on limite fortement les dommages photochimiques (altérations chimiques causées par la lumière) et le stress cellulaire (perturbation du fonctionnement normal de la cellule).
- Observation au long cours : il devient possible de suivre des processus biologiques (ensembles de réactions et dynamiques dans les systèmes vivants) sur de longues durées sans perturber significativement le métabolisme (ensemble des réactions chimiques nécessaires au fonctionnement d’un organisme) de l’échantillon.
Comparaison entre des images de microscopie à super-résolution RESOLFT et des images de microscopie confocale de cellules CV-1. Les cellules sont marquées avec des anticorps ciblant :
(A) la vimentine, (B) l’α-tubuline et (C) la protéine Nup153 (composant du pore nucléaire). (D) Profils d’intensité de fluorescence mesurés le long des lignes indiquées en (A–C) : microscopie confocale (bleu clair) et RESOLFT (rouge). Les profils (1–3) correspondent à une moyenne de cinq lignes adjacentes, perpendiculaires aux structures observées. L’écart entre deux lignes correspond à la taille d’un pixel.
Échelle : 1 µm
Crédits : Ilgen P. et al., 2015, PLoS ONE.
Avec une résolution spatiale de l’ordre de 20 à 50 nanomètres, la microscopie RESOLFT montre qu’à l’échelle du nanomonde, ce n’est pas la puissance lumineuse brute qui prime, mais le contrôle fin et la réversibilité des états de fluorescence (capacité d’une molécule à passer de manière répétable entre un état fluorescent et non fluorescent). Une approche où la précision et la subtilité remplacent la force.
La fin de l'invisible
Ces instruments ont fait de la lumière un outil presque chirurgical, non pas en contournant les lois de la physique, mais en les exploitant jusqu’à leurs limites. Le prix Nobel de 2014 a marqué une rupture nette. Depuis, le mouvement ne cesse de s’accélérer.
Le levier ne se situe plus uniquement dans les lentilles (éléments optiques qui focalisent et dirigent la lumière), mais de plus en plus dans les algorithmes.
L’intelligence artificielle reconstruit l’image là où l’optique s’arrête, isole des structures subcellulaires (organisations internes plus petites que la cellule) noyées dans le bruit de fond (signaux parasites), et restitue des informations à l’échelle nanométrique en temps réel. Elle ne se contente plus d’assister l’observation.
Quand l’optique s’interrompt, la vision humaine se prolonge dans le calcul et redessine les contours mouvants de l’invisible.
Article précédent de Les instruments de l'invisible